電子配置と分子軌道
電子配置と分子軌道は、化学において原子や分子の性質を理解するために不可欠な概念です。電子がどのように配置され、分子内でどのように相互作用するかを知ることで、物質の化学的性質や反応性を予測することができます。この記事では、電子配置と分子軌道について詳しく解説し、それぞれの概念がどのように化学反応や分子の性質に影響を与えるのかを説明します。
電子配置とは?
電子配置とは、原子内の電子がどのように配置されているかを示したものです。電子は、原子核の周りにあるエネルギー準位(軌道)に従って配置されており、特定のルールに基づいて軌道を埋めていきます。電子配置を理解することは、原子の化学的性質や結合性を理解するための基本です。
ボーアモデルとエネルギー準位
原子内の電子は、異なるエネルギー準位に存在し、それぞれのエネルギー準位には特定の軌道が含まれています。電子が占めるエネルギー準位は、内側から外側へ向かうにつれてエネルギーが高くなります。最も内側のエネルギー準位には2個までの電子が入り、次に進む準位には8個の電子が入ります。この電子配置のパターンは、パウリの排他原理やフントの規則に従っています。
電子配置のルール
電子が軌道にどのように配置されるかを決定する基本的なルールがいくつかあります。
- パウリの排他原理: 1つの軌道には最大2個の電子しか存在できず、その電子は異なるスピン状態(+1/2と-1/2)を持ちます。
- フントの規則: 同じエネルギー準位に複数の軌道が存在する場合、まずは各軌道に1個ずつ電子が入ります。その後、必要に応じて2個目の電子が同じ軌道に入ります。
- アウフバウの原理: 電子はエネルギーの低い軌道から順番に配置されます。これにより、安定した電子配置が得られます。
例えば、酸素原子の電子配置は、1s2 2s2 2p4という形式で表されます。ここで、1s²は1番目のエネルギー準位(s軌道)に2個の電子が配置されていることを示し、2s2は2番目のエネルギー準位のs軌道に2個、2p4は2番目のエネルギー準位のp軌道に4個の電子が配置されていることを示しています。
電子配置と周期表
原子の電子配置は、周期表の構造と密接に関連しています。周期表の各列(族)は、最外殻電子の配置が似ている元素を含み、これにより似た化学的性質を持ちます。例えば、アルカリ金属(第1族)はすべて最外殻に1個の電子を持ち、これが強い反応性の一因となっています。同様に、貴ガス(第18族)は最外殻が満たされており、非常に安定で反応性が低いです。
分子軌道とは?
分子軌道は、複数の原子が結合して分子を形成するときに、原子軌道が組み合わさってできる新しい軌道です。分子軌道理論では、原子の電子がもともと占めていた原子軌道が、分子全体にわたる新しい軌道(分子軌道)を形成し、これが分子全体の電子配置を決定します。
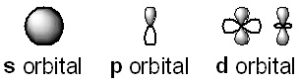
分子軌道の形成
分子軌道は、複数の原子の原子軌道の線形結合によって形成されます。この過程では、結合軌道と反結合軌道が生成されます。
- 結合軌道: 原子軌道が相互作用し、分子を安定化させる軌道です。エネルギーが低く、原子間で電子が共有されることで結合が形成されます。
- 反結合軌道: エネルギーが高く、原子軌道が反発することで分子を不安定化させる軌道です。反結合軌道に電子が入ると、結合が弱まり、場合によっては分子が解離します。
分子軌道のエネルギー準位図
分子軌道はエネルギー準位の違いによって区別され、これをエネルギー準位図で表すことができます。例えば、2つの水素原子が結合して水素分子(H2)を形成する際、各水素原子の1s軌道が結合して分子軌道が形成されます。
- 2つの1s軌道が結合して、1つの結合軌道(σ1s)と1つの反結合軌道(σ*1s)が生成されます。
- σ1s軌道にはエネルギーが低い電子が入り、安定な結合を形成します。一方、σ*1s軌道にはエネルギーの高い電子が入らないため、結合が安定化します。
σ結合とπ結合
分子軌道は、原子軌道の相互作用の形式によってσ結合とπ結合に分類されます。
- σ結合(シグマ結合): 原子軌道が頭同士で重なり合って形成される最も強い結合です。単結合はすべてσ結合で構成されます。
- π結合(パイ結合): 原子軌道が側面で重なり合って形成される結合で、σ結合に比べて弱いです。二重結合や三重結合では、σ結合とともにπ結合が関与します。
例えば、エチレン(C2H4)の分子では、2つの炭素原子間に1つのσ結合と1つのπ結合が存在し、二重結合が形成されています。
電子配置と分子軌道の関係
電子配置と分子軌道は、原子や分子の化学的性質を理解するために不可欠です。電子配置が原子の化学的性質を決定する一方、分子軌道は分子の安定性や反応性を決定します。
化学結合の形成
電子配置に基づいて、どのように原子同士が結合するかが決まります。最外殻電子が他の原子と共有されることで共有結合が形成され、その際に原子軌道が分子軌道に再編成されます。分子軌道のエネルギー準位に応じて、結合の強さや長さが決まり、分子の物理的・化学的性質に影響を与えます。
分子の反応性
分子の反応性は、分子軌道の配置に依存しています。結合軌道が満たされている場合、分子は比較的安定ですが、反結合軌道が占有されると、分子は反応しやすくなります。また、電子が存在する最高被占軌道(HOMO)と、電子を受け取る最低空軌道(LUMO)のエネルギー差は、分子の反応性や電子の移動に影響を与えます。このエネルギー差が小さいほど、分子は反応しやすくなります。
分子軌道理論の応用
分子軌道理論は、化学反応や物質の性質を理解するために幅広く応用されています。たとえば、有機化学や材料科学では、分子軌道を使って新しい化合物の設計や予測が行われています。また、量子化学においては、分子軌道を計算して物質の性質を理論的に解析することが可能です。
結論
電子配置と分子軌道は、原子や分子の性質を理解する上で非常に重要な概念です。電子配置は、原子の化学的性質や反応性を決定し、分子軌道は分子全体の安定性や反応性に大きく関与します。これらの概念を理解することで、化学反応のメカニズムや物質の特性をより深く知ることができ、新しい物質や材料の設計にも役立ちます。
\さらに有機化学を学びたい方はコチラ/







