アシロイン縮合【Acyloin Condensation】

アシロイン縮合(Acyloin Condensation)は、有機合成において炭素-炭素結合を形成する重要な手法の一つです。特に環化反応としても利用され、主に中環および大環の構築に非常に効果的です。
概要
- アルカリ金属(通常はナトリウム)を触媒として使用し、エステル化合物同士をカップリングしてアシロイン(α-ヒドロキシケトン)を生成する
- 特に環状化合物の合成において有効で、5員環から大環に至るまで、さまざまな環構造を形成するために使用される
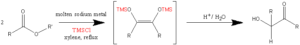
- 2分子の脂肪族エステルを熱キシレン中、高度に分散した融解ナトリウム金属で処理することによってアシロインを得る手法
- 生成したアシロインのジナトリウム誘導体を酸性にすると、合成中間体として有用なアシロインが遊離する
- 脂肪族のモノエステルは対称化合物を与えるが、ジエステルは環状アシロインを与える
- 分子内アシロイン縮合は10員環以上の閉環反応として最も優れた手法の一つであり、今までに34員環まで合成されている
- 芳香族アシロインの合成には、2つの芳香族アルデヒド間のベンゾイン縮合が適用される
- アシロインやそのアニオンは酸化されやすいため、アシロイン縮合は不活性ガス雰囲気下で行われる
- 小員環を合成する場合、TMSClを共存させて超音波を使用すると収率が向上する。これは、TMSClを加えることで、β-脱離、Claisen縮合、Dieckmann縮合のような塩基触媒の副反応を抑えることができるためである
- 生成したビスシロキシアルケンは単離するか、加水分解や加アルコール分解によってアシロインに変換する。
歴史
更新をお待ちください。
反応機構
アシロイン縮合は、エステル基がナトリウムによって還元され、カルボン酸塩を経てラジカル中間体が生成されることから始まります。その後、生成されたラジカルが他のエステル分子と結合して新しい炭素-炭素結合を形成し、最終的にアシロインが生成されます。
この反応の特徴は、ラジカル機構が関与する点であり、特に中環および大環の環化において非常に効率的であることが知られています。
実験手順
更新をお待ちください。
発展
小環および通常サイズの環(5~7員環)
5員環および6員環の合成において、アシロイン縮合は非常に効果的です。例えば、2-ヒドロキシシクロペンタノンや2-ヒドロキシシクロヘキサノンのような基本的な環構造が簡便に合成されます。
中環(8~11員環)
中環の合成は、通常他の手法では難しいですが、アシロイン縮合はこのサイズの環を高収率で合成する方法として特に有効です。この反応は、8員環や10員環のアシロイン誘導体の合成に広く利用されています。
大環およびマクロ環
12員環以上の大環の合成においても、アシロイン縮合は有力な方法の一つです。例えば、マクロサイクルムスク(香料成分)などの合成に応用されており、通常の手法では得られにくい大環状化合物を効率よく生成できます。
応用例
J. Salaunによるアシロイン縮合の改良
J. Salaunらは、超音波により促進されるアシロイン縮合の研究を行った。
彼らは、1,4-、1,5-、1,6-ジエステルのアシロインカップリングにより、四、五、六員環生成物が得られることを見出した。
β-クロロエステルがTMSCl存在下に三員環に環化する反応では、当初は高度に分散したナトリウムを必要としたが、超音波による反応活性化により改良された。
S. Sieburthによるトリシクロデカン基本骨格の合成
Anopterus種のジテルペンアルカロイドは、アノプテリン (anopterine) を主成分とし、高い抗腫瘍活性を示す。
このアルカロイドのすべてがトリシクロ[3.3.21,4.0]デカンを基本骨格を含んでいる。
S. Sieburthらは、この三員環骨格の短工程構築にアシロイン縮合を鍵反応として用いた。
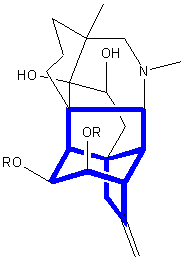 アノプテリン
アノプテリンD. J. Burnellによる二環性ジケトンの合成
D. J. Burnellらは、アセタールにつながった環状アシロインをLewis酸により促進されるジェミナルアシル化に付すことによって、二環性ジケトン (bicyclic diketones) を合成した。
ここで必要なビスシロキシアルケンは、通常のアシロイン縮合により得られる。
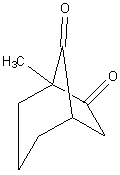 二環性ジケトン
二環性ジケトン参考文献
<Original Publication>
Bouveault, L.; Loquin, R. Compt. Rend. 1905, 140, 1593.
<Review>
K. Thomas Finley, “The Acyloin Condensation as a Cyclization Method”, Chem. Rev., 1964, 64 (5), 573–589. DOI: 10.1021/cr60231a004
<Related Publication>
関連書籍







